Ciclo dell’azoto in acquario? Pure voi?
Sì, pure noi di Acquario.top – ma garantiamo che troverai qualcosa in più del solito, leggendo quello che segue 😉
Cosa non troverai in questo articolo
- lo schemino “ammonio → nitriti → nitrati“
- il mese di maturazione (quando capiremo cosa voglia dire, forse lo integreremo)
- battute con nitriti e cavalli come protagonisti
- fonti delle informazioni discutibili
Iniziamo.
Alcune definizioni prima di cominciare
Seguono alcune brevi definizioni (senza pretesa di esaustività) per comprendere meglio di cosa si parla nell’articolo ed evitare di farvi aprire pagine di Wikipedia mentre leggete 😀
- Composto organico: composto che contiene al suo interno atomi di carbonio legati ad altri elementi con legami covalenti (praticamente quasi tutti gli elementi con carbonio all’interno, non sono molte le eccezioni: cianuri, bicarbonati e carburi).
- Organismo Autrotrofo: organismo che usa, come fonte di energia, composti non organici e, come fonte di carbonio, carbonati e CO2. Esempio: piante.
- Organismo Eterotrofo: organismo che usa, come fonte di energia e di carbonio, composti organici. Esempi: animali, uomo.
- Organismo Aerobico: organismo che usa l’ossigeno per la respirazione (come accettore di elettroni). Esempi: animali, uomo, alcuni batteri.
- Organismo Anaerobico: organismo che usa elementi diversi dall’ossigeno per la respirazione (composti dell’azoto, manganese, ferro, solfati, composti organici). Esempio: alcuni batteri.
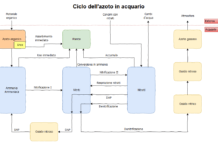
Ciclo dell’azoto in acquario
Quello dell’azoto è uno dei tanti cicli presenti in acquario, poiché più o meno ogni elemento ne ha uno: abbiamo il ciclo del carbonio, del fosforo e di altri elementi.
Tuttavia, soprattutto per le conseguenze, spesso nefaste, è il ciclo dell’azoto ad influenzare maggiormente gli acquariofili, anche quelli che lo ignorano (i pesci morti due-tre settimane dall’inserimento vorrebbero poter confermare…).
Poiché si tratta di un ciclo, potremmo cominciare da un punto qualsiasi di esso: per esempio, da quel che mettiamo in acquario.
L’azoto organico in acquario
Cos’è?
L’azoto organico è quello che troviamo legato ad atomi di carbonio. Lo possiamo trovare sostanzialmente in tre posti:
- nei mangimi e in generale in tutti gli alimenti (vivi, freschi, surgelati, liofilizzati etc) che diamo ai pesci;
- nei materiali in decomposizione (feci, legni, foglie, fibre vegetali in genere, pesci o invertebrati morti etc);
- nei fertilizzanti per piante d’acquario, solitamente come urea.
POC e DOC
Questa materia organica si decompone in componenti sempre più piccole, dette POC (Particulate Organic Carbon – Carbonio Organico in Particelle), fino a diventare così piccole da essere disciolte (DOC – Dissolved Organic Carbon – Carbonio Organico Dissolto).
Probabilmente abbiamo visto tutti del POC negli acquari: è quella sorta di melma o detrito che si deposita solitamente sul fondo, in cui passano, se presenti, lumache e altri invertebrati.
Il DOC, invece, non è visibile, a meno di un suo accumulo (non dannoso), che si manifesta con un ingiallimento dell’acqua.

Dove va?
L’azoto organico viene subito attaccato da ceppi batterici eterotrofi (e altri organismi), che decompongono l’azoto organico in composti inorganici, ovvero privi del carbonio. Con questo processo – detto mineralizzazione – si ha usualmente la produzione di ammoniaca (NH3) e di anidride carbonica (CO2), come prodotti di scarto.
I batteri responsabili di questo processo sono eterotrofi ma possono essere sia aerobici, sia anaerobici.
Un primo passaggio del ciclo dell’azoto è quindi il seguente:
Azoto organico → Ammoniaca + CO2
Per quanto riguarda la sola urea, le piante possono riuscire ad assorbirne direttamente una parte, prima che inizi a venire decomposta.
Una parte dell’azoto organico, invece, viene usata dai batteri stessi per le loro strutture e metabolismo interni.
L’ammonio e l’ammoniaca in acquario
Cosa sono?
L’ammoniaca è uno dei principali e più pericolosi inquinanti negli acquari.
È prodotta direttamente dal metabolismo dei pesci o decomposta dai batteri a partire dai composti organici dell’azoto oppure, infine, inserita come fertilizzante (solitamente come ammonio: nitrato di ammonio, fosfato di ammonio etc).
La tossicità dell’ammoniaca è dipendente principalmente dal pH dell’acqua, poiché il pH può trasformare l’ammoniaca nel comunque tossico, ma in misura inferiore, ammonio.
La reazione di equilibrio è la seguente:
NH4+ + OH– ↔ NH4OH ↔ NH3 + H2O
che ci dice che in acqua sono sempre presenti sia ammoniaca (NH3) sia ione ammonio (NH4+). Tuttavia al variare del pH possiamo praticamente azzerare la concentrazione di ammoniaca, più tossica.
Come varia la percentuale di ammoniaca ed ammonio?
Nel dettaglio, la percentuale di ammoniaca scende allo scendere del pH.
A pH 6.3 circa, l’ammoniaca è lo 0.1% contro il 99.9% dell’ammonio.
All’aumentare del pH, la percentuale di ammoniaca aumenta rapidamente: già a pH 8, l’ammoniaca supera il 3% rispetto al 97% di ammonio.
A pH 9.25 si ha metà ammoniaca e metà ammonio.
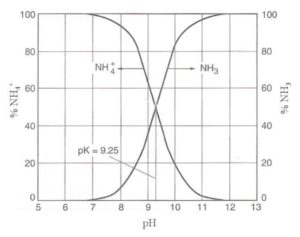
Indicativamente, c’è circa una variazione delle percentuali di ordine 10 per ogni punto di pH (e di ordine 100 ogni due punti e così via).
Ad esempio, se il pH scende da 8 a 7, la concentrazione di ammonio aumenta dallo 0.33% circa al 3.3% (e quella dell’ammoniaca scende dal 99.7% al 96.6% circa).
Per inciso, questo è uno dei motivi per cui le variazioni devono essere fatte lentamente. Un punto di pH può alterare le concentrazioni di ammoniaca di 10 volte!
Dove vanno?
L’ammonio e l’ammoniaca possono venire assorbiti facilmente da piante ed alghe, se presenti, e da batteri nitrificanti.
Le piante e le alghe possono, infatti, usare l’ammonio come fonte di azoto a rapida assimilazione, pronto da usare subito. Non possono infatti accumulare l’ammonio per usarlo in un secondo tempo.
Come spiegato da Diana Walstad e dagli studi da ella citati, l’ammonio è assorbito come forma di azoto preferenziale dalla maggior parte delle piante.
L’ammonio e l’ammoniaca non assorbiti da piante ed alghe vengono invece trasformati, da alcuni ceppi batterici aerobici autotrofi (Nitrosomonas e archeobatteri ossidatori dell’ammonio), in nitriti, secondo la reazione:
NH4+ + ½O2 → 2H+ + NO2– + H2O
I nitriti in acquario
Cosa sono?
I nitriti derivano dall’ossidazione (aggiunta di ossigeno) di ammonio e ammoniaca ed è il primo di due passi della nitrificazione.
I nitriti sono estremamente tossici (più dell’ammonio) per i pesci, poiché i nitriti hanno la capacità di legarsi all’emoglobina contenuta nel sangue impedendo a quest’ultima di portare l’ossigeno. L’effetto è simile a quello delle intossicazioni da monossido di carbonio nell’uomo.
Infatti, uno degli effetti principali di basse concentrazioni di nitriti è proprio quello della difficoltà respiratoria: pesci che hanno respiro accelerato o tentano di respirare sul pelo dell’acqua, boccheggiando.
Se la concentrazione di nitriti aumenta per un tempo sufficientemente lungo, la morte dei pesci non è da escludere, anzi. Non ho le statistiche sotto mano, ma a naso direi che i nitriti siano fra le prime cause di morte negli acquari, specialmente in quelli appena allestiti.
Dove vanno?
I nitriti possono venire assorbiti dalle piante (dalle alghe in misura minore se non nulla, purtroppo non ci sono molti studi a riguardo), ma la maggior parte è convertita in nitrati da altri ceppi batterici, sempre aerobici e autotrofi (Nitrospira), secondo la reazione:
NO2– + ½O2 → NO3–
I nitrati in acquario
Cosa sono?
I nitrati derivano dall’ossidazione dei nitriti e sono il risultato del secondo dei due passi di cui è composta la nitrificazione.
Possono anche essere introdotti mediante vari fertilizzanti comunemente usati, quali nitrati di potassio, calcio, magnesio, ammonio etc.
I nitrati non sono tossici per i pesci a basse concentrazioni, tuttavia al crescere della concentrazione possono iniziare a dare problemi. Problemi non nel senso che il pesce muore (a differenza dell’accumulo di nitriti), quanto piuttosto a disturbi nel comportamento (riproduttività, attività) e nella crescita, anche a livello di sviluppo delle pinne e colorazione.
Per alcuni pesci, sono consigliabili livelli di nitrati il più bassi possibili (se non misurabili, anche meglio), mentre altri pesci sono un po’ più tolleranti – non significa però che abbiano piacere di nuotare nei nitrati… Torneremo su questo con più dettagli in seguito.
Continuiamo col ciclo dell’azoto!
Dove vanno?
I nitrati vengono assorbiti dalle piante, insieme o in sostituzione all’ammonio. Per le piante, infatti, è oneroso l’assorbimento dei nitrati poiché lo devono riconvertire in ammonio, per poterlo utilizzare direttamente. Tuttavia per le piante sono importanti anche i nitrati, poiché possono accumularli nei tessuti per utilizzarli in un secondo momento (cosa che non possono fare con l’ammonio).
Oltre a venire assorbiti dalle piante, i nitrati possono venire convertiti in azoto gassoso (N2) da parte di alcuni batteri anaerobici.
Se invece volessimo ascoltare una tanta parte di acquariofili, l’unico modo efficace di rimuovere i nitrati è quello di fare cambi d’acqua, anche se non sempre risolvono (e anche su questo torneremo).
Il ciclo dell’azoto in acquario “modello classico” si concluderebbe qui, ma non è finita!
Ci sono ancora varie pagine di informazioni e non abbiamo ancora nominato la maturazione…